Vergiftungen mit Pilzen gehören zu den seltenen Vergiftungen, nehmen in den vergangenen Jahren jedoch kontinuierlich zu.1 Tödliche Pilzvergiftungen können oft mit rechtzeitiger Behandlung abgewendet werden, so dass wir euch in diesem vor dem Höhepunkt der Pilzsaison um die 39. KW2 noch einmal auf den aktuellen Stand bringen möchten.
Aufgrund der vielen verschiedenen Pilzarten gibt es eine große Zahl an Vergiftungsbildern.
Da eine umfassende Übersicht den Rahmen dieses Formats sprengen würde, möchten wir in diesem Artikel die häufigsten zehn bei Anfragen zu Pilzvergiftungen in Deutschland konsumierten Pilzarten mit ihren Vergiftungsbildern besprechen und darüber hinaus das allgemeine Vorgehen bei vermuteten Pilzvergiftungen vorstellen.
Wer noch Interesse an sehr seltenen Vergiftungssyndromen hat, wird im Bedarfsfall in der Giftnotrufzentrale beraten oder in einem Artikel von White und Kollegen fündig, in dem ein (äußerst komplexer) Algorithmus zum symptomorientierten Identifizieren von fast allen Pilzvergiftungen erläutert wird.3 Wer sich hingegen gar nicht lange mit Pilzvergiftungen aufhalten will, sollte zumindest das Phalloides-Syndrom erkennen und zu diesem Abschnitt springen.
Risikoabschätzung
Die Risikoabschätzung bei möglicher Pilzvergiftung ist selbst für Experten schwierig. Das liegt zum einen daran, dass oft Mischpilzgerichte mit mehr als einer Art von Pilzen gegessen werden, sodass unter Umständen nur ein einziger giftiger Pilz verwechselt und konsumiert wurde. Zum anderen äußern sich echte und auch unechte Pilzvergiftungen zunächst meist mit Magen-Darm-Beschwerden, sodass die Erstsymptomatik nur begrenzt zur Einordnung hilft.
Echt oder unecht?
Generell sollte zwischen echten Pilzvergiftungen und unechten Pilzvergiftungen unterschieden werden. Bei der echten Pilzvergiftung führen auch durch ausreichendes Garen nicht inaktivierte Toxine zu einem reproduzierbaren Krankheitsbild, solange eine ausreichende Dosis konsumiert wurde.
Bei der unechten Pilzvergiftung kommt es hingegen aufgrund dessen, dass Pilze allgemein schwer verdaulich sind (Mühlendahl beschreibt einen Fall, in dem ein Patient nach dem extensiven Konsum von Pfifferlingen einen mechanischen Ileus erlitt und laparatomiert werden musste4), die konsumierten Pilze verdorben waren oder nicht ausreichend lange gegart wurden, zu GI-Beschwerden. Auch allergische Reaktionen sind möglich.4,5
Identifikation
Um das Eintrittsrisiko einer Vergiftung und deren potenziellen Verlauf einschätzen zu können, ist es entscheidend, die konsumierten Pilze zu identifizieren. Hierzu können Pilzsachverständige über die Giftinformationszentralen oder direkte Kontaktaufnahme aktiviert werden, die aus Resten der Mahlzeit oder teils auch aus Erbrochenem die konsumierte Pilzart oder Pilzarten identifizieren.
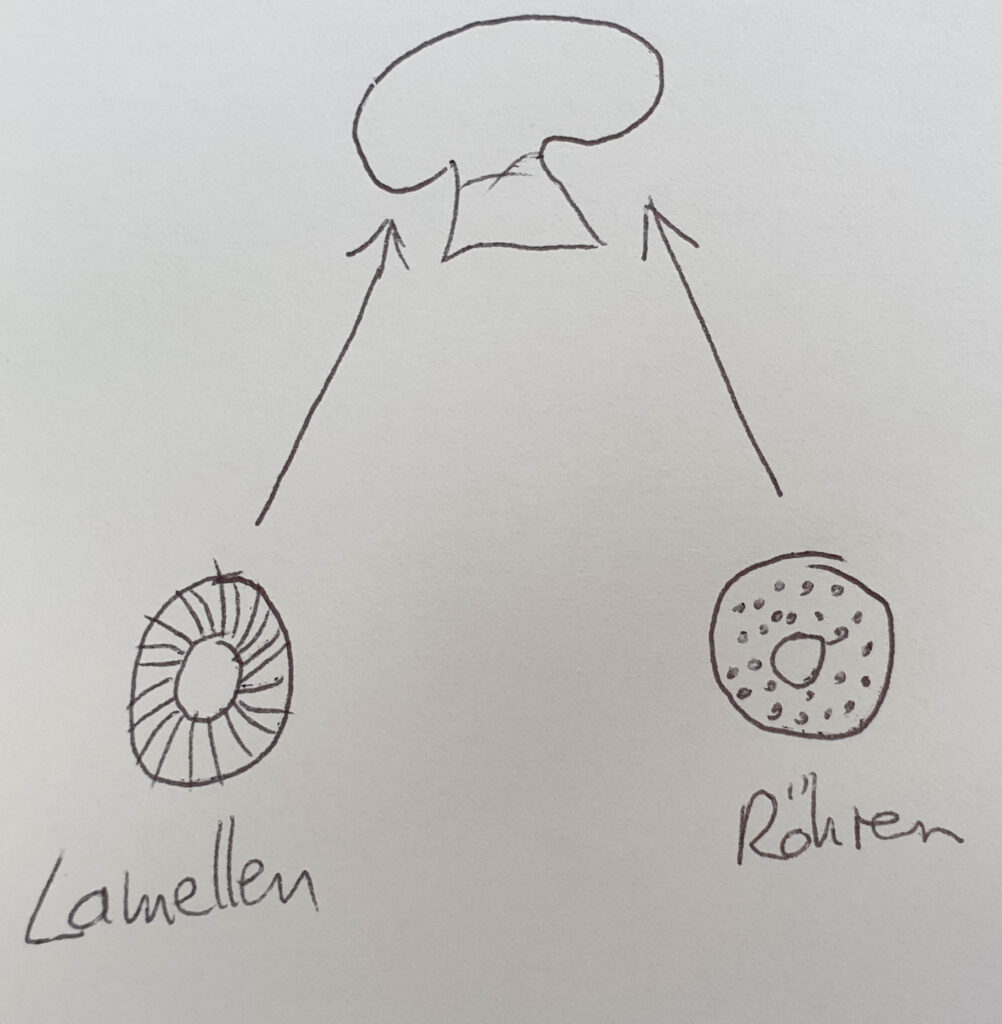
Als einfache Faustregel für den pilzunkundigen Behandler kann es helfen, zu fragen, ob vom Patienten Röhren- oder Lamellenpilze gesammelt wurden. Vereinfacht und fachlich nicht ganz korrekt gesagt, haben Röhrenpilze an der Unterseite des Pilzhutes Röhren (ein typischer Vertreter ist der Steinpilz), während bei Lamellenpilzen hier Lamellen zu finden sind. Wurden ausschließlich Röhrenpilze gesammelt sind, ist im schlimmsten Fall nur mit ausgeprägten gastroenteritischen Symptomen zu rechnen. Bei Lamellenpilzen können jedoch schwere Vergiftungsbilder auftreten.4,5
Eine zweite Faustregel besagt, dass bei Auftreten von gastroenteritischen Beschwerden erst nach mehr als 6 Stunden nach einer Pilzmahlzeit mit einer gefährlichen Intoxikation zu rechnen ist, während eine kürzere Latenzzeit meist bei harmlosen echten oder unechten Pilzvergiftungen vorkommt. Dennoch können natürlich in einem Mischpilzgericht auch ein Pilz, der früh gastrointeritische Beschwerden auslöst, und ein Knollenblätterpilz, der diese erst später und dann ein Leberversagen auslöst, gemeinsam enthalten sein.
Rein statistisch gesehen sind unechte Pilzvergiftungen („Pilzunverträglichkeitssyndrom“) und gastrointestinale Pilzsyndrome mit etwa 80 % aller Pilzvergiftungen deutlich am häufigsten vertreten.5
Häufige Pilzintoxikationen und ihre Syndrome in Deutschland
Die Datenlage zur Anzahl von Pilzvergiftungen in Deutschland ist aufgrund eines fehlenden zentralen Registers für Vergiftungen leider dünn. Eine Auswertung aus dem Jahr 2006 mit Daten von fünf der neun deutschen Giftinformationszentralen und des BfR zeigte folgende 10 Pilzarten als häufigste Auslöser (die hier typischen Syndrome haben wir ergänzt):6
- Knollenblätterpilze 5,1 % der Fälle (Phalloides-Syndrom mit Leberversagen)
- „Magic Mushrooms“ 4 % der Fälle (Psilocybin (=Halluzinogenes)-Pilzsyndrom)
- Karbol-Champignon (=Gift-Egerling, Karbolerglinge) 3,4 % der Fälle (gastrointestinales Pilzsyndrom)
- Hallimasch 2% der Fälle (Pilzunverträglichkeitssyndrom, falls nicht genug gegart)
- Pantherpilze 2% der Fälle (Pantherpilzsyndrom)
- Fliegenpilze 2 % der Fälle (Pantherpilzsyndrom
- Gallenröhrlinge 1,7 % der Fälle (auffällig bitter, gastrointestinales Pilzsyndrom)
- Düngerlinge 1,4 % der Fälle (divers, führend halluzinogenes und/oder gastrointestinales Pilzsyndrom)
- Kahle Kremplinge 1,0 % der Fälle (gastrointestinales Pilzsyndrom, sehr selten Paxillus-Syndrom)
- Satanspilze 0,9 % der Fälle (gastrointestinales Pilzsyndrom)
Bemerkenswert dabei ist, dass durch die Top Ten der Pilzvergiftungen nur eine von vier Pilzvergiftungen erklärt werden kann, was nochmal das große Spektrum der auslösenden Pilze und die Schwierigkeit der Pilzidentifikation unterstreicht.
Welche Syndrome sind nun bei diesen Top 10 häufig?
Syndrome mit kurzer Latenzzeit (≤ 6 Stunden)
Das Pilzunverträglichkeitssyndrom oder die unechte Pilzintoxikation ist keine Intoxikation im eigentlichen Sinne. Es tritt beim Konsum von nicht durchgegarten eigentlich essbaren oder verdorbenen Pilzen, oder aufgrund individueller physiologischer Faktoren mit gastrointestinalen Symptomen wie Blähungen, Übelkeit, Brechdurchfall auf.
Klassische Auslöser sind z.B. Hallimasche (z.B. Armillaria mellea) und der Perlpilz (Amanita rubescens). Eine Garzeit von mindestens 20 Minuten sollte generell beachtet werden.5
Das gastrointestinale Pilzsyndrom hingegen ist eine echte Intoxikation und wird durch Pilze, die sowohl roh als auch korrekt gegart giftig sind ausgelöst. Häufig sind hier vor allem im Rheintal der Karbolchampignon oder der Satanspilz, die sich auch in der Top 10 Liste befinden, aber auch der Riesenrötling, Tigerritterling und Kartoffelbovist4 oder die schon gefährlich nach abdominellen Symptomen klingenden Pilze wie die Bauchwehkoralle oder der Speitäubling.5
Schwere Verläufe sind hier selten und äußern sich durch massive Hypovolämie und Elektrolytstörungen. Die Therapie ist symptomatisch.4,5
Das Psilocybin- oder halluzinogene Pilzsyndrom wird meist durch nicht einheimische, getrocknet verkaufte und unter dem Begriff „magic mushrooms“ bekannte Pilze ausgelöst. Typische Sorten sind der Blauende Düngerling, der Kubanische Kahlkopf und der Mexikanische Kahlkopf. Meist weniger starke Formen werden durch einheimisch vorkommende und beim Sammeln verwechselte Kahlköpfe oder einige Düngerling-Arten ausgelöst.5 Dabei bleibt der Konsum von 1-2 einheimischen Pilzen von der Wiese oder Weideflächen bei Kleinkindern wohl immer symptomlos, nicht jedoch der Konsum von von den Eltern stibitzter getrockneter Varianten, die bei Kleinkindern häufig schwere Angstzustände und Halluzinationen auslösen.4
Beim Erwachsenen kommt es nach etwa 20 Minuten durch Psilocybin und Psilocin zu einer LSD-ähnlichen Wirkung.5 Diese hält typischerweise für 2-6 Stunden an, milde Nebenwirkungen wie Schlafstörungen können bis zu 12 Stunden persistieren.7 Klassische Psychosen sind dabei eher untypisch,3 vielmehr kommt es zu Synästhesien, verstärkten Farben, teils verwaschenem Sehen und einem Gefühl der Depersonalisation mit Verlust und Raum- und Zeitgefühl. Etwa jeder dritte Konsument erlebt auch Angstgefühle bis hin zu starker Paranoia. In den Niederlanden wurden einige Todesfälle von Konsumenten beschrieben, die unter Einfluss von Magic mushrooms (wohl im Glauben, fliegen zu können) aus dem Fenster sprangen.7 Mühlendahl beschreibt als weitere Wirkung noch Benommenheit, Ataxie und muskuläre Hypotonie sowie selten Bradykardien und Hypotonien.4 Typisch sind aber (eher milde) sympathomimetische Effekte mit Tachykardie, Mydriasis und so weiter.5 Selten scheint es als chronische Nebenwirkung zu Flashbacks an den Rauschzustand zu kommen.7
Therapeutisch bleibt die symptomatische Therapie mit Benzodiazepinen.4 Antipsychotika würden wir nur als Rescue-Medikation einsetzen bei anders nicht kontrollierbarer massiver Psychose.
Das Pantherpilz- oder Fliegenpilz-Syndrom wird typischerweise vom Fliegenpilz (Amanita muscaria), Pantherpilz (Amanita pantherina) – der dem essbaren Perlpilz zum Verwechseln ähnlich sieht – und dem Königsfliegenpilz (Amanita regalis) ausgelöst. Die hierin enthaltenen Toxine (v.a. Muscimol und Ibotensäure) interagieren mit diversen zentralen Neurotransmittern. Hierdurch kommt es zu einer wechselnden Symptomatik, die zeit- und dosisabhängig führend cholinerg- oder anticholinerg ist.5
Nach 30 Minuten bis 3 h kommt es zu (laut Mühlendahl an den Alkoholrausch erinnernden) Rauschzuständen mit Halluzinationen sowie Angstzuständen, die sich mit Phasen von Bewusstseinsminderung und Bewusstlosigkeit abwechseln. Darüber hinaus sind gastrointestinale Symptome (Erbrechen/Durchfall), Hypotonie, Ataxie und Krampfanfälle möglich.5 Bradykardie und Erbrechen sind dabei eher selten und psychotische, angstbesetzte Halluzinationen im Wechsel mit Bewusstseinstrübungen vor allem im schweren Verlauf zu finden.4 Die Symptomatik zeigt sich nach etwa 12 Stunden komplett regredient und es kommt teils zu tiefem Schlaf.4
Therapeutisch sollten wieder führend Benzodiazepine eingesetzt werden, wobei Haloperidol bei psychotischen Zuständen gut zu wirken scheint.4 Die Empfehlungen zur Gabe von Physostigmin und Atropin sind in der Literatur nicht eindeutig. Aufgrund der oftmals zwischen cholinerger und anticholinerger Wirkung wechselnden Symptomatik wären wir hier jedoch zurückhaltend. Wir würden eher Mühlendahls Empfehlung folgen, kein Physostigmin einzusetzen und Atropin nur bei schwerer Bradykardie einzusetzen.4
Der kahle Krempling wurde lange Zeit als essbar betrachtet und führt bei unzureichender Garung zum gastrointestinalen Pilzsyndrom.8 Allerdings werden in der Literatur in den letzten Jahren immer wieder Fälle von immunhämolytischer Anämie, DIC und Multiorganversagen nach mehrfachem Konsum des kahlen Kremplings beschrieben. Hierbei handelt es sich um das wohl sehr seltene Paxillus-Syndrom.4,5 Stöver und Kollegen konnten im Jahr 2019 14 solcher Fallberichte finden.8 Es scheint bei wenigen Menschen, die vielleicht aufgrund von Genetik oder Vorerkrankungen besonders empfindlich hierfür sind, nach wiederholtem, bis dahin problemlosem Konsum des Kahlen Kremplings zu einer Antigen-Antikörper-Reaktion zu kommen.
Vermutet wird, dass es zu einer massenhaften Antikörperfreisetzung auf ein Pilzantigen kommt und der Antigen-Antikörper-Komplex sich auf den Erythrozyten ablagert. So wird eine Autoimmunhämolyse mit allen Konsequenzen auslöst. Die Latenzzeit beträgt dabei ungefähr 2 Stunden.
Im Gegensatz zum gastrointestinalen Pilzsyndrom, das normalerweise alle Beteiligten der Pilzmahlzeit betrifft, ist hier meist nur ein Konsument betroffen, und ein rascher Anstieg des Bilirubins kann helfen, eine Abgrenzung zum Phalloides-Syndrom zu treffen. Die Sterblichkeit des Paxillus-Syndroms scheint hoch zu sein und die Therapie muss auf der Intensivstation erfolgen. Dabei ist die symptomatische Therapie führend, lediglich eine Plasmapherese wird bisher therapeutisch vorgeschlagen.5,8
Das Muskarin-Syndrom wird (nicht, wie der Name Amanita muscaria vermuten lässt,) durch den Fliegenpilz, sondern durch einige Risspilze wie den Ziegelroten Risspilz (Inocybe erubescens), Trichterlinge oder manche Helmlinge (z. B. Mycena rosea) ausgelöst. Das Muskarin aktiviert dabei die muskarinergen Acetylcholinrezeptoren des parasympathischen Nervensystems und wirkt somit als Parasympathomimetikum. Es kann die Bluthirnschranke jedoch nicht überschreiten und wirkt somit nur peripher. Die Latenzzeit ist mit 30 bis 120 Minuten kurz, hiernach kommt es zu Miosis, Hypersalivation und Schweißausbrüchen sowie Durchfall und Erbrechen, seltener auch zu Bradykardien. Als Antidot kann Atropin in 1-2 mg-Schritten (bzw. 0,02 mg/kg bei Kindern) intravenös gegeben werden, bis die Symptomatik sistiert.5
Die für Kleinkinder typische Aufnahme nur eines Risspilzes verursacht meist keine Vergiftungserscheinungen.4
Syndrome mit langer Latenzzeit ≥ 6 Stunden
Das Phalloides- oder Amanita-/Amatoxin-Syndrom bei der Knollenblätterpilzvergiftung ist das wohl wichtigste Syndrom, da fast alle tödlichen Pilzvergiftungen hierauf zurückzuführen sind.5 Ohne Möglichkeit der Lebertransplantation liegt die Sterblichkeit mit oder ohne Antidot um 10 beziehungsweise 20%.9 Praktisch jährlich werden Todesfälle in Deutschland beschrieben. Besonders tückisch ist, dass ein einziger Pilz in einer Pilzmahlzeit genug Amatoxin enthält, um mehrere Personen lebensgefährlich zu vergiften, und dass der eigentlich in Nadel- und Mischwäldern vorkommende Pilz auch auf Lichtungen in städtischen Parks wächst, wo er für Kleinkinder erreichbar ist. Für diese kann auch nur ein Bissen bereits tödlich sein.4
Ausgelöst wird das Syndrom fast immer durch den grünen Knollenblätterpilz (Amanita phalloides), aber der spitzkegelige (teils auch „weiße“) Knollenblätterpilz (Amanita virosa), der Gifthäubling (Galerina marginata, gerne verwechselt mit dem schmackhaften Stockschwämmchen, Kuehneromyces mutabilis) und der fleischbräunliche Giftschirmling enthalten ebenfalls Amatoxine. Diese blockieren im Zellkern die RNA-Polymerase II und damit die DNS-Transkription mit klinisch führendem Leberzellschaden.5
Die Symptome verlaufen ähnlich der Paracetamol-Vergiftung triphasisch. Nach meist 10-12 Stunden (6-24 h) Latenzzeit kommt es zu wässrigen, teils choleraähnlichen Diarrhoen, heftigem Erbrechen und abdominellen Krämpfen für oft 6-9 Stunden,5 die jedoch bis zu 36 Stunden anhalten können.3,4 In einer anschließenden Phase der trügerischen Remission mit klinischer Besserung für circa 2 Tage kommt es bereits etwa 24 Stunden nach Konsum zum zunächst asymptomatischen Anstieg der Leberwerte (v.a. Transaminasen steigend und Quick fallend). Bei entsprechender Dosis mit fulminantem Leberversagen wird ab dem vierten Tag das Leberversagen klinisch apparent. Hier zeigt sich Blutungsneigung und im schwersten Verlauf Kreislaufversagen, am 5. Tag eine beginnende hepatische Enzephalopathie und am 6. Tag kommt es typischerweise zum hepatischen Koma und Nierenversagen mit Tod am 7. bis 10. Tag., wenn keine Lebertransplantation erfolgt.4
Kommt es nicht zum fulminanten Leberversagen, erreichen die Transaminasen etwa am 3. Tag ihr Peak und fallen dann meist ab dem vierten Tag.10
Zur Diagnosesicherung kann Urin in Speziallabore verschickt werden. Das Ergebnis hat jedoch mehr forensischen Charakter und darf nicht den Therapiebeginn verzögern.
Therapeutisch wird sich zu Nutze gemacht, dass Amatoxin über einen hohen enterohepatischen Kreislauf verfügt. Eine Unterbrechung dieses „Teufelskreises“ wird durch repetitive Kohlegabe und eine reduzierte hepatozytäre Wiederaufnahme durch das Antidot Silibinin angestrebt. Dosiert wird letzteres mit 5mg/kg über eine Stunde und anschließend 20 mg/kg/24h.5 Die Indikation zur Antidot-Gabe richtet sich nach der Phase der Vorstellung.
Bereits in der Latenzphase sollte im Verdachtsfall repetitiv Kohle gegeben und mit der Antidottherapie begonnen werden. Bleibt eine gastrointestinale Phase dann aus, kann die Antidottherapie nach 30 Stunden beendet werden.5
Bei Vorstellung erst in der gastrointestinalen Phase, sollte ebenfalls repetitiv Aktivkohle gegeben und Silibinin verabreicht werden. Außerdem sollte die Aufnahme auf eine Intensivstation erfolgen und auf eine ausreichende Diurese geachtet werden, um die glomeruläre Filtration der Amatoxine möglichst aufrecht zu erhalten. Falls nach 72 Stunden die Transaminasen normal sind, kann die Antidotgabe beendet werden,5 ansonsten sollte sie weitergeführt werden bis die Transaminasen deutlich fallen und der Quick-Wert ansteigt.4
Die Datenqualität für die Antidot-Therapie mit Silibinin sind mäßig (unter anderem fehlen RCTs), die Sterblichkeit scheint jedoch in einem Review von Saller und Kollegen mit Antidottherapie bei etwa 10% versus 18 % ohne Antidottherapie zu liegen.9 Alternativ kann auch Penicillin gegeben werden (0,3-1 Mio I.E./kgKG/24h bis maximal 40 Mio IE/24h) bis Silibinin, welches wirksamer zu sein scheint, verfügbar ist.4,5,11 Teils wird auch ACC zusätzlich empfohlen, die Datenlage unterstützt das bisher jedoch nicht.11,12
Kommt es trotz Antidottherapie zum fulminanten Leberversagen, ist die Lebertransplantation der einzig noch mögliche kurative Therapieansatz. Die Kriterien, wann genau transplantiert werden sollte, (z.B. Kings-College-Kriterien oder Score nach Ganzert13) werden in der Literatur kritisch diskutiert und sind nicht eindeutig. Eine gute Übersicht über die verschiedenen Argumente und Übersicht über die Literatur liefert hier im Falle des Falles der Artikel von Karvellas und Kollegen, die von 13 Patienten mit Amatoxin-induziertem Leberversagen berichten, von denen 6 spontan ohne Lebertransplantation und 5 nach Lebetransplantation überlebten, wohingegen 2 Patienten ohne Lebertransplantation verstarben.14
Grob gesagt deuten ein Quick-Wert von ≤ 20% und eine fehlende Besserung der Leberwerte am vierten Tag mit ausgeprägtem akuten Nierenversagen auf eine Transplantationsnotwendigkeit hin.4
Es scheint auch eine besondere Form mit hyperdynamem Kreislaufversagen an Tag 2-4 zu geben, welche auf Rehydratation und Katecholamine nicht anspricht. Hier sollte bereits vor dem Erreichen des hepatischen Komas eine Lebertransplantation angestrebt werden.4
Es gibt noch diverse weitere Syndrome nach Pilzvergiftungen, wie das Coprinus-Syndrom, das durch Alkoholkonsum bei Konsum entsprechender Pilze entsteht, das Gyromitrin-Syndrom mit Bewusstseinsminderung und Leberversagen, das Orellanus-Syndrom mit Nierenversagen nach Tagen bis Wochen oder die in der Literatur noch diskutierte Rhabdomyolyse mit teils konsekutivem Nierenversagen beim Konsum bestimmter Tricholoma-Arten. Hier bieten neben den Giftzentralen White und Kollegen3 oder auch die Deutsche Gesellschaft für Mykologie eine gute Übersicht über die zu erwartende Symptomatik.
Wer sich für Pilzvergiftungen mit einhergehendem Nierenversagen interessiert, sei auf dieses Review von Beaumier verwiesen.15
Management
Ein Patient stellt sich in Arztpraxis, Notaufnahme oder dem Rettungsdienst mit einer Ingestion möglicherweise toxischer Pilze oder bereits klinisch apparenten Pilzvergiftung vor. Wie sollte man nun allgemein vorgehen?
Folgendes Vorgehen würden wir nach Empfehlungen von Romanek und Mühlendahl vorschlagen:4,5
Als erstes sollte gefragt werden, ob eine gastrointestinale Symptomatik ≥ 6 Stunden nach der (ersten) Pilzmahlzeit aufgetreten ist. Wird dies bejaht, muss von einem Phalloides-Syndrom ausgegangen und der Patient entsprechend behandelt werden.
Darüber hinaus sollte versucht werden die konsumierten Pilze, ggf. auch aus Resten von Erbrochenem oder der Pilzmahlzeit, zu identifizieren. Neben dem Hinzuziehen von Pilzsachverständigen per eigenständiger Recherche oder Kontaktaufnahme mit einem Giftnotruf sollte gefragt werden, ob Röhrenpilze (eher harmlose gastrointestinale Beschwerden zu erwarten) oder Lamellenpilze (schwere Vergiftungen möglich) konsumiert wurden.
Sind die Patienten symptomatisch und die Einnahme liegt nur kurz (≤ 1h) zurück, sollte Aktivkohle gegeben werden.
Bleibt die Situation unklar, sollte die Indikation zur stationären Überwachung und ggf. auch Antidottherapie großzügig gestellt werden, da insbesondere beim Mischpilzgericht trotz einer kurzen Latenzzeit bis zum Symptombeginn (z.B. durch nicht korrekt gegarte andere Pilze) eine Vergiftung mit einem amatoxinhaltigen Pilz nicht ausgeschlossen werden kann.5
Wurden die Pilze sicher identifiziert, sollten entsprechende spezifische Maßnahmen – soweit möglich – getroffen werden.
Kommt es zur Einnahme eines Pilzes beim Kleinkind, ist diese meist harmlos, jedoch können auch schon kleine Mengen eines Knollenblätterpilzes hier gefährlich werden und dieser auch an Rändern innerstädtischer Parks oder Garten gefunden werden, sodass der Pilz immer identifiziert und erst hiernach Maßnahmen ergriffen werden sollten. Meist werden aber eher harmlose Pilze wie der Heudüngerling auf Wiesen, der Glimmertingling an Baumstümpfen oder der gelbe Faltenschirmling aus dem Blumentopf konsumiert.4
Als unbedenklich zu werten sind Fälle, in denen sehr geringe Pilzmengen geschluckt wurden (deutlich unter 1 cm3). Auch das alleinige Berühren oder Ablecken, oder der Kontakt mit einem Giftpilz im Sammelkorb können als harmlos betrachtet werden.5
Zusammenfassung
- Es existieren viele verschiedene Vergiftungsbilder nach Pilzkonsum. Der Großteil besteht aus unangenehmen, jedoch selten gefährlichen Brechdurchfällen und Magen-Darm-Beschwerden durch echte oder unechte Pilzvergiftung
- Als Faustregel führen Röhrenpilze „nur“ zu gastrointestinalen Vergiftungen, während Lamellenpilze die schwerer toxischen Arten beinhalten
- Vergiftungen mit dem Amatoxin-haltigen Knollenblätterpilz führen zum Phalloides-Syndrom mit teils fulminantem Leberversagen und enden nicht selten tödlich
- Besonders beim Auftreten von Brechdurchfällen mehr als 6 Stunden nach einer Pilzmahlzeit muss unbedingt an dieses Syndrom gedacht und eine Therapie mit repetitiver Kohlegabe und Silibinin-Gabe eingeleitet werden
- Pilzsachverständigen gelingt es oftmals, die Pilze zu identifizieren und eine spezifische Therapie festzulegen
- Bleibt die Lage unklar, sollte die Indikation zur stationären Aufnahme, Laborkontrolle und ggf. Antidotgabe eher großzügig gestellt werden, um keine Amatoxin-Vergiftung zu übersehen
Das Vorgehen stichpunktartig zusammengefasst findet ihr auch als Pocket Card zum Download hier.
Wenn euch dieser Artikel gefallen hat, ihr etwas vermisst oder Themenwünsche für weitere Artikel habt, schreibt uns an christoph [at] toxdocs.de Wir freuen uns über euer Feedback! Bei Facebook und in unserem RSS-Feed werdet ihr über neue Posts auf dem laufenden gehalten.
Quellen
1. Ärzteblatt DÄG Redaktion Deutsches. Viele Notrufe wegen Pilzvergiftungen. Deutsches Ärzteblatt. Published October 14, 2019. Accessed September 9, 2020. https://www.aerzteblatt.de/nachrichten/106647/Viele-Notrufe-wegen-Pilzvergiftungen
2. Schenk-Jäger KM, Egli S, Hanimann D, Senn-Irlet B, Kupferschmidt H, Büntgen U. Introducing Mushroom Fruiting Patterns from the Swiss National Poisons Information Centre. PLOS ONE. 2016;11(9):e0162314. doi:10.1371/journal.pone.0162314
3. White J, Weinstein SA, De Haro L, et al. Mushroom poisoning: A proposed new clinical classification. Toxicon. 2019;157:53-65. doi:10.1016/j.toxicon.2018.11.007
4. von Mühlendahl KE. Vergiftungen Im Kindesalter. 4th ed. Georg Thieme Verlag; 2003.
5. Romanek K, Haberl B, Pfab R, Stich R, Eyer F. Pilzvergiftungen: Symptome, Diagnostik und Therapie. Notfall + Rettungsmedizin. 2016;19(4):301-314. doi:10.1007/s10049-016-0151-z
6. Hahn, Axel. Pilzvergiftungen in Deutschland. Presented at the: 23.03 2012; Berlin. Accessed September 9, 2020. https://www.bfr.bund.de/cm/343/pilzvergiftungen-in-deutschland.pdf
7. Amsterdam J van, Opperhuizen A, Brink W van den. Harm potential of magic mushroom use: A review. Regulatory Toxicology and Pharmacology. 2011;59(3):423-429. doi:10.1016/j.yrtph.2011.01.006
8. Stöver A, Haberl B, Helmreich C, et al. Fatal Immunohaemolysis after the Consumption of the Poison Pax Mushroom: A Focus on the Diagnosis of the Paxillus Syndrome with the Aid of Two Case Reports. Diagnostics. 2019;9(4):130. doi:10.3390/diagnostics9040130
9.Saller R, Meier R, Brignoli R. The Use of Silymarin in the Treatment of Liver Diseases. Drugs. 2001;61(14):2035-2063. doi:10.2165/00003495-200161140-00003
10.Ward J, Kapadia K, Brush E, Salhanick SD. Amatoxin Poisoning: Case Reports and Review of Current Therapies. The Journal of Emergency Medicine. 2013;44(1):116-121. doi:10.1016/j.jemermed.2012.02.020
11. Enjalbert F, Rapior S, Nouguier-Soulé J, Guillon S, Amouroux N, Cabot C. Treatment of amatoxin poisoning: 20-year retrospective analysis. J Toxicol Clin Toxicol. 2002;40(6):715-757. doi:10.1081/clt-120014646
12. Diaz JH. Amatoxin-Containing Mushroom Poisonings: Species, Toxidromes, Treatments, and Outcomes. Wilderness & Environmental Medicine. 2018;29(1):111-118. doi:10.1016/j.wem.2017.10.002
13. Ganzert M, Felgenhauer N, Zilker T. Indication of liver transplantation following amatoxin intoxication. J Hepatol. 2005;42(2):202-209. doi:10.1016/j.jhep.2004.10.023
14. Karvellas CJ, Tillman H, Leung AA, et al. Acute liver injury and acute liver failure from mushroom poisoning in North America. Liver International. 2016;36(7):1043-1050. doi:10.1111/liv.13080
15. Beaumier M, Rioult J-P, Georges M, Brocheriou I, Lobbedez T, Lanot A. Mushroom Poisoning Presenting With Acute Kidney Injury and Elevated Transaminases. Kidney International Reports. 2019;4(6):877-881. doi:10.1016/j.ekir.2019.02.016
